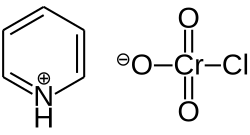
Chlorochromian pirydyny
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
C5H6ClCrNO3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
C5H5NHClCrO3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molowa |
215,56 g/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd |
pomarańczowy krystaliczny proszek[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||||||||||||
Chlorochromian pirydyny, PCC, odczynnik Coreya – organiczny związek chemiczny, sól pirydyniowa kwasu chlorochromowego. Jest utleniaczem stosowanym w syntezie chemicznej do utleniania alkoholi do aldehydów oraz ketonów.
Otrzymywanie
Odczynnik ten został opisany w roku 1975 przez Eliasa Jamesa Coreya i Williama Suggsa w 1975 roku[3]. Został on otrzymany przez przypadek – zamiast planowanego związku chromu(V) Suggs użył związku chromu(VI)[4]. Typowa procedura obejmuje reakcję pirydyny z kwasem chlorochromowym, uzyskanym z tlenku chromu(VI) i 6 M kwasu solnego. Reakcje prowadzi się w temperaturze pokojowej w dichlorometanie (DCM) przez około 1–2 godziny[5].
Zastosowanie
PCC stosowany jest jako utleniacz grupy hydroksylowej alkoholi pierwszo- i drugorzędowych do aldehydów i ketonów[6][7][8]. Utlenianie alkoholi pierwszorzędowych. prowadzone w DCM kończy się na etapie aldehydu, natomiast w przypadku użycia DMF jako rozpuszczalnika zachodzi utlenianie do kwasów karboksylowych[5].
Alternatywnym odczynnikiem o podobnej reaktywności, lecz mniejszej kwasowości jest dichromian pirydyny (odczynnik Cornfortha)[5].
Przypisy
- 1 2 3 4 Chlorochromian pirydyniowy (nr 190144) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2012-06-21]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Chlorochromian pirydyny (nr 190144) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2012-06-21]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ E.J. Corey, J. William Suggs, Pyridinium Chlorochromate. An Efficient Reagent for Oxidation of Primary and Secondary Alcohols to Carbonyl Compounds, „Tetrahedron Letters”, 16 (31), 1975, s. 2647–2650, DOI: 10.1016/S0040-4039(00)75204-X.
- ↑ J. Suggs, The Old Stuff. In the Pipeline [online], pipeline.corante.com, 12 października 2005 [zarchiwizowane z adresu 2015-09-05].
- 1 2 3 Pyridinium Chlorochromate (PCC). Organic Chemistry Portal. [dostęp 2014-12-15].
- ↑ Leo A. Paquette, Martyn J. Earle, Graham F. Smith, (4''R'')-(+)-''tert''-Butyldimethylsiloxy-2-cyclopenten-1-one, „Organic Syntheses”, 73, 1996, s. 36, DOI: 10.15227/orgsyn.073.0036.
- ↑ Yong Tu i inni, Synthesis of 1,2:4,5-di-O-isopropylidene-D-erythro-2,3-hexodiulo-2,6-pyranose. A highly enantioselective ketone catalyst for epoxidation, „Organic Syntheses”, 80, 2003, s. 1, DOI: 10.15227/orgsyn.080.0001.
- ↑ James D. White, Uwe M. Grether, Chang-Sun Lee, (R)-(+)-3,4-Dimethylcyclohex-2-en-1-one, „Organic Syntheses”, 82, 2005, s. 108, DOI: 10.15227/orgsyn.082.0108.