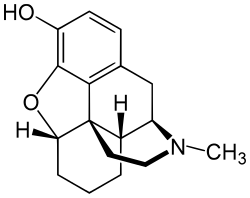
Dezomorfina
| |||||||||||||||
| |||||||||||||||
| Ogólne informacje | |||||||||||||||
| Wzór sumaryczny |
C17H21NO2 | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
271,35 g/mol | ||||||||||||||
| Wygląd |
prostokątne płytki po krystalizacji z mieszaniny acetonu i wody[1] | ||||||||||||||
| Identyfikacja | |||||||||||||||
| Numer CAS | |||||||||||||||
| PubChem | |||||||||||||||
| DrugBank | |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||
| Klasyfikacja medyczna | |||||||||||||||
| Legalność w Polsce | |||||||||||||||
Dezomorfina – organiczny związek chemiczny, pochodna morfiny, różniąca się od niej brakiem grupy hydroksylowej i wiązania podwójnego. Ma działanie uspokajające i przeciwbólowe, jest ok. 8–10 razy silniejsza od morfiny[3][4][5][6]. Tradycyjnie syntetyzowana z kodeiny[7].
Dezomorfina została opisana i opatentowana w 1932 roku w Stanach Zjednoczonych[8]. Stała się popularna w Rosji w 2010 roku, gdzie jest otrzymywana domowymi sposobami z mieszaniny m.in. kodeiny, jodu i fosforu. Uzyskany w ten sposób narkotyk, tzw. krokodyl (ros. крокодил), ze względu na zanieczyszczenia i toksyczne związki powstałe w procesie produkcji, nieodwracalnie uszkadza organizm zażywającego, na skórze którego pojawiają się zielonkawe plamy spowodowane gniciem ciała. Po pewnym czasie występują również niegojące się rany, w które często wdaje się gangrena, doprowadzając do śmierci albo do konieczności amputacji mięśnia (o ile nie został on wcześniej dostatecznie zniszczony, aby nastąpiło samoistne oderwanie się od ścięgien i kości)[9][10].
Synteza
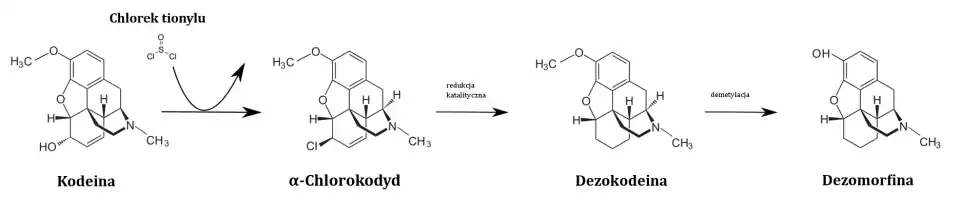
- Synteza dezomorfiny z kodeiny
Przypisy
- 1 2 3 4 Desomorphine, [w:] Merck Index. An Encyclopedia of Chemicals, Drugs, and Biologicals, wyd. 14, Whitehouse Station, New Jersey: Merck & Company, 2006, ISBN 978-0-911910-00-1, OCLC 938242785 (ang.).
- ↑ Desomorphine, [w:] ChemIDplus [online], United States National Library of Medicine [dostęp 2016-08-11] (ang.).
- ↑ Alan F. Casy, Robert T. Parfitt, Opioid Analgesics. Chemistry and Receptors, New York: Plenum Press, 1986, s. 32, ISBN 978-0-306-42130-3.
- ↑ R. Bognar, S. Makleit, Neue Methode für die Vorbereitung von dihydro-6-desoxymorphine, „Arzneimittelforschung”, 8 (6), 1958, s. 323–325, PMID: 13546093 (niem.).
- ↑ Paul A.J. Janssen, A Review of the Chemical Features Associated with Strong Morphine-Like Activity, „British Journal of Anaesthesia”, 34 (4), 1962, s. 260–268, DOI: 10.1093/bja/34.4.260, PMID: 14451235.
- ↑ Lewis J. Sargent, Everette L. May, Agonists-antagonists derived from desomorphine and metopon, „Journal of Medicinal Chemistry”, 13 (6), 1970, s. 1061–1063, DOI: 10.1021/jm00300a009, PMID: 4098039 (ang.).
- ↑ Nathan B. Eddy, Homer A. Howes, Studies of Morphine, Codeine and their Derivatives X. Desoxymorphine-C, Desoxycodeine-C and their Hydrogenated Derivatives, „Journal of Pharmacology and Experimental Therapeutics”, 55 (3), 1935, s. 67–257 (ang.).
- ↑ Lyndon Frederick Small, Morphine Derivative and Processes for its Preparation, patent US 1980972, 13 listopada 1932 [dostęp 2012-01-21] (ang.).
- ↑ Michał Siegieda, „Krokodyl” wygryzł heroinę, [w:] TVP Info [online], 9 stycznia 2012 [zarchiwizowane z adresu 2012-04-15].
- ↑ Kamil Przybyliński, „Krokodyl”, niezwykle groźny narkotyk z Rosji coraz popularniejszy, [w:] Wiadomości24.pl [online], 9 stycznia 2012 [zarchiwizowane z adresu 2012-01-13].
![]() Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.