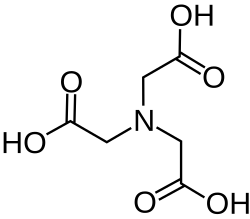
Kwas nitrylotrioctowy
|
|
| Nazewnictwo |
|
|
| Inne nazwy i oznaczenia |
| NTA (z ang. nitrilotriacetic acid), tris(karboksymetylo)amina, N,N-bis(karboksymetylo)glicyna |
|
| Ogólne informacje |
| Wzór sumaryczny |
C6H9NO6 |
| Masa molowa |
191,14 g/mol |
| Wygląd |
biały lub prawie biały, krystaliczny proszek[1] |
| Identyfikacja |
| Numer CAS |
139-13-9 |
| PubChem |
8758 |
| DrugBank |
DB03040 |
| SMILES |
|
C(C(=O)O)N(CC(=O)O)CC(=O)O |
|
|
|
|
|
| Podobne związki |
| Podobne związki |
EDTA, EGTA, TAED |
Jeżeli nie podano inaczej, dane dotyczą
stanu standardowego (25 °C, 1000 hPa) |
Kwas nitrylotrioctowy (NTA) – organiczny związek chemiczny stosowany powszechnie jako ligand chelatowy tworzący kompleksy z takimi kationami jak: Ca2+
, Cu2+
czy Fe3+
. Ma podobne zastosowanie jak EDTA, jednak jest bardziej przyjazny dla środowiska, gdyż znacznie łatwiej ulega biodegradacji.