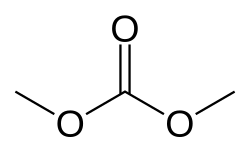
Węglan dimetylu
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
C3H6O3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
(CH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molowa |
90,08 g/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd |
bezbarwna ciecz | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Węglan dimetylu – organiczny związek chemiczny, ester metanolu i kwasu węglowego będący przezroczystą cieczą o charakterystycznym zapachu. Otrzymywany jest w reakcji metanolu z fosgenem, której produktami są węglan dimetylu i chlorowodór:
- 2CH
3OH + COCl
2 → (CH
3O)
2C=O + 2HCl
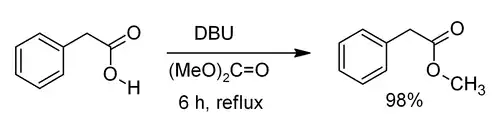
Wykorzystywany jest jako substrat w przemyśle farmaceutycznym, przy produkcji farb oraz agrochemikaliów. Jest łagodnym i nietoksycznym środkiem metylującym[8] pochodne aniliny, fenolu i kwasy karboksylowe, reakcja wymaga jednak stosunkowo wysokiej temperatury (autoklaw) lub użycia silnie zasadowego DBU[9]:
Przypisy
- 1 2 3 4 5 6 Haynes 2014 ↓, s. 3-206.
- 1 2 Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- 1 2 3 4 5 6 7 8 9 Dimethyl carbonate (nr 517127) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2016-04-13]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- 1 2 3 Haynes 2014 ↓, s. 6-63.
- 1 2 Węglan dimetylu, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2016-04-13] (ang.).
- ↑ Węglan dimetylu (nr 517127) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2016-04-13]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Haynes 2014 ↓, s. 16-20.
- ↑ Pietro Tundo, Maurizio Selva. The Chemistry of Dimethyl Carbonate. „Accounts of Chemical Research”. 35 (9), s. 706–716, 2002. DOI: 10.1021/ar010076f.
- ↑ Wen-Chung Shieh, Stephen Dell, Oljan Repič. Nucleophilic Catalysis with 1,8-Diazabicyclo[5.4.0]undec-7-ene (DBU) for the Esterification of Carboxylic Acids with Dimethyl Carbonate. „The Journal of Organic Chemistry”. 67 (7), s. 2188–2191, 2002. DOI: 10.1021/jo011036s.
Bibliografia
- CRC Handbook of Chemistry and Physics, William M. Haynes (red.), wyd. 95, Boca Raton: CRC Press, 2014, ISBN 978-1-4822-0867-2 (ang.).