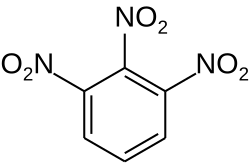
1,2,3-Trinitrobenzen
|
|
| Nazewnictwo |
|
|
| Nomenklatura systematyczna (IUPAC) |
1,2,3-trinitrobenzen |
|
| Ogólne informacje |
| Wzór sumaryczny |
C6H3N3O6 |
| Masa molowa |
213,11 g/mol |
| Identyfikacja |
| Numer CAS |
603-13-4 |
| PubChem |
521922 |
| SMILES |
|
C1=CC(=C(C(=C1)[N+](=O)[O-])[N+](=O)[O-])[N+](=O)[O-] |
|
| InChI |
|
InChI=1S/C6H3N3O6/c10-7(11)4-2-1-3-5(8(12)13)6(4)9(14)15/h1-3H |
| InChIKey |
ONOWMDPHGJEBAZ-UHFFFAOYSA-N |
|
|
|
|
|
| Podobne związki |
| Podobne związki |
1,3,5-trinitrobenzen, 1,2,4-trinitrobenzen |
Jeżeli nie podano inaczej, dane dotyczą
stanu standardowego (25 °C, 1000 hPa) |
1,2,3-Trinitrobenzen – organiczny związek chemiczny z grupy nitrozwiązków, trinitrowa pochodna benzenu. Ma dwa izomery podstawienia: 1,3,5-trinitrobenzen i 1,2,4-trinitrobenzen.
Można go otrzymać w wyniku utleniania 2,6-dinitroaniliny lub 2,6-dinitrofenylohydroksyloaminy, np. za pomocą 98% H
2O
2 w stęż. H
2SO
4 lub kwasem trifluoronadoctowym (CF
3COOOH)[4].
Wykazuje nietypowo wysoką reaktywność w substytucji nukleofilowej grupy 2-nitrowej przez anilinę w porównaniu do 1,2,4-trinitrobenzenu. Przypisuje się to efektom sterycznym związanym ze stłoczeniem 3 grup nitrowych i związanym z tym ich odchyleniem od płaszczyzny pierścienia i ich słabszemu sprzężeniu z pierścieniem[4].
Przypisy
- ↑ W.W. Borsche W.W., Über β-Nitroaryl-hydroxylamine: I. β-2.4- und β-2.6-Dinitrophenyl-hydroxylamin, „Berichte der deutschen chemischen Gesellschaft (A and B Series)”, 56 (6), 1923, s. 1494–1501, DOI: 10.1002/cber.19230560639 (niem.).
- ↑ R.E.R.E. Parker R.E.R.E., T.O.T.O. Read T.O.T.O., 607. The mechanism of displacement reactions. Part III. Kinetics of the reactions of the four 2-halogeno-1,3-dinitrobenzenes and 1,2,3-trinitrobenzene with aniline in ethanol, „Journal of the Chemical Society”, 1962, s. 3149–3153, DOI: 10.1039/JR9620003149 (ang.).
- ↑ A.F.A.F. Holleman A.F.A.F., F.E. vanF.E. Haeften F.E. vanF.E., Les Six Trichloronitrobenzènes et Les Trois Trinitrobenzènes; Leur Réaction Avec le Méthylate de Sodium, „Recueil des Travaux Chimiques des Pays-Bas”, 40 (2), 1921, s. 67–98, DOI: 10.1002/recl.19210400202 (fr.).
- 1 2 Arnold T.A.T. Nielsen Arnold T.A.T. i inni, Synthesis of polynitro compounds. Peroxydisulfuric acid oxidation of polynitroarylamines to polynitro aromatics, „Journal of Organic Chemistry”, 45 (12), 1980, s. 2341–2347, DOI: 10.1021/jo01300a015 (ang.).