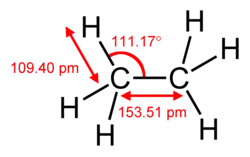
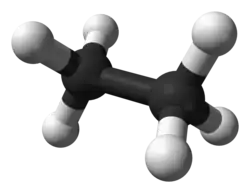
Etan
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
C2H6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
30,07 g/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd |
bezbarwny, bezwonny gaz | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pochodne nienasycone | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
Etan (C2H6) – organiczny związek chemiczny z grupy alkanów. Występuje w przyrodzie jako jeden ze składników gazu ziemnego.
Otrzymywanie
Na skalę techniczną jest otrzymywany z produktów obróbki termicznej ropy naftowej i węgla kamiennego. Do celów laboratoryjnych można go otrzymać w wyniku elektrolizy stężonego roztworu soli octanowej (np. octanu sodu):
- 2CH
3COO−
→ C
2H
6↑ + 2CO
2↑ + 2e−
albo przez katalityczne uwodornienie etenu lub etynu (np. na katalizatorze platynowym):
- C2H4 + H2 → C2H6
- C2H2 + 2H2 → C2H6
W wyniku katalitycznego odwodornienia etanu otrzymuje się eten (etylen), który jest ważnym surowcem w przemyśle chemicznym (np. do produkcji polietylenu). Odwodornienie odbywa się przeważnie na katalizatorze niklowym.
Przypisy
- 1 2 3 4 Ethane, [w:] ChemIDplus [online], United States National Library of Medicine [dostęp 2012-08-08] (ang.).
- 1 2 Etan (nr 00582) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski.
- 1 2 3 Ethane, [w:] PubChem [online], United States National Library of Medicine, CID: 6324 (ang.).
- 1 2 Etan, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2015-04-10] (ang.).
- ↑ Etan (nr 00582) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych.