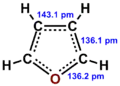
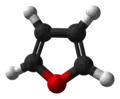
Furan
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
C4H4O | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
68,07 g/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd |
przezroczysta, bezbarwna ciecz o intensywnym zapachu[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pochodne | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Furan, furfuran – heterocykliczny związek chemiczny z endocyklicznym atomem tlenu, cykliczny eter[6] o charakterze aromatycznym.
Jest znacznie bardziej reaktywny w substytucji elektrofilowej niż benzen. Podstawienie elektrofilowe zachodzi głównie w pozycji 2 w stosunku do atomu tlenu. W środowisku kwasowym polimeryzuje.
W warunkach normalnych jest bezbarwną cieczą o słodkawym zapachu chloroformu[4]. Jest dobrze rozpuszczalny w etanolu i eterze dietylowym. Otrzymuje się go z furfuralu działaniem pary wodnej na katalizatorze tlenkowym. Stosowany jest do produkcji kwasu adypinowego i heksametylenodiaminy.
Przypisy
- 1 2 3 4 5 6 7 8 9 10 11 Furan. The Chemical Database. Wydział Chemii Uniwersytetu w Akronie. [dostęp 2012-08-28]. (ang.).[niewiarygodne źródło?]
- 1 2 Furan (nr 185922) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski.
- 1 2 3 Furan, [w:] ChemIDplus [online], United States National Library of Medicine [dostęp 2012-08-28] (ang.).
- 1 2 Podręczny słownik chemiczny, Romuald Hassa (red.), Janusz Mrzigod (red.), Janusz Nowakowski (red.), Katowice: Videograf II, 2004, s. 141, ISBN 83-7183-240-0.
- 1 2 Furan, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2015-04-10] (ang.).
- ↑ Mallikharjuna, Rao L., Yousuf, Syed Khalid, Mukherjee, Debaraj, Taneja, Subhash Chandra. Regioselective azidotrimethylsilylation of carbohydrates and applications thereof. „Organic & Biomolecular Chemistry”. 10 (45), s. 9090–9098, 2012. DOI: 10.1039/C2OB26324F.