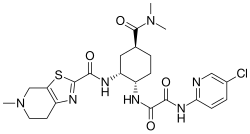
Edoksaban
| ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||
| Wzór sumaryczny |
C24H30ClN7O4S | |||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
548,06 g/mol | |||||||||||||||||||||||||||
| Wygląd |
biały lub jasno żółty krystaliczny proszek[1] | |||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||
| Numer CAS | ||||||||||||||||||||||||||||
| PubChem | ||||||||||||||||||||||||||||
| DrugBank | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||
| Klasyfikacja medyczna | ||||||||||||||||||||||||||||
| ATC | ||||||||||||||||||||||||||||
| Stosowanie w ciąży |
kategoria C[3] | |||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
Edoksaban (łac. edoxabanum) – wielofunkcyjny organiczny związek chemiczny, lek przeciwzakrzepowy, bezpośredni i odwracalny inhibitor czynnika Xa, stosowany w zapobieganiu zakrzepom u pacjentów z grup wysokiego ryzyka.
Mechanizm działania
Edoksaban jest bezpośrednim i odwracalnym inhibitorem czynnika Xa[4]. Poprzez zahamowanie czynnika Xa oraz protrombinazy zapobiega wytwarzaniu trombiny i poprzez to powstawaniu skrzepu[4].
Metabolizm
Edoksaban jest metabolizowany w niewielkim stopniu, w drodze hydrolizy przez karboksyesterazę, sprzęgania oraz oksydacji przez CYP3A4/5[5].
Zastosowanie
Unia Europejska
- zapobieganie udarom mózgu i zatorowości systemowej u dorosłych pacjentów z niezastawkowym migotaniem przedsionków z co najmniej jednym czynnikiem ryzyka, takim jak przebyty udar mózgu lub przemijający napad niedokrwienny (ang. transient ischaemic attack, TIA), wiek ≥ 75 lat, nadciśnienie tętnicze, cukrzyca, zastoinowa niewydolność serca (klasa wg NYHA ≥ II)[4],
- leczenie zakrzepicy żył głębokich oraz zatorowości płucnej u dorosłych[4],
- zapobieganie zakrzepicy żył głębokich oraz zatorowości płucnej u dorosłych[4].
Stany Zjednoczone
- zmniejszenie ryzyka wystąpienia udaru mózgu i zatorowości systemowej u pacjentów z migotaniem przedsionków niezwiązanym z wadą zastawkową[3]
Edoksaban znajduje się na wzorcowej liście podstawowych leków Światowej Organizacji Zdrowia (WHO Model Lists of Essential Medicines) (2019)[6].
Edoksaban jest dopuszczony do obrotu w Polsce (2020)[7].
Działania niepożądane
Edoksaban może powodować następujące działania niepożądane u ponad 1% pacjentów: niedokrwistość, krwawienie z nosa, krwawienie z przewodu pokarmowego, krwiomocz, nudności, krwiak, krwawienie z pochwy u kobiet poniżej 50 roku życia, świąd, wysypka oraz zwiększenie aktywności bilirubiny i γ-glutamylotranspeptydazy w osoczu[4].
Dawkowanie
Zalecane dawkowanie edoksabanu[4]:
- w zapobieganiu udarom mózgu i zatorowości obwodowej u dorosłych pacjentów z migotaniem przedsionków niezwiązanym z wadą zastawkową z jednym lub kilkoma czynnikami ryzyka, takimi jak zastoinowa niewydolność serca, nadciśnienie tętnicze, wiek ≥ 75 lat, cukrzyca, udar lub przemijający napad niedokrwienny w wywiadzie – 60 mg jeden raz na dobę,
- w leczeniu zakrzepicy żył głębokich oraz zatorowości płucnej – 60 mg jeden raz na dobę, po terapii lekiem przeciwzakrzepowym podawanym pozajelitowo przez co najmniej 5 dni,
- w zapobieganiu zakrzepicy żył głębokich oraz zatorowości płucnej – 60 mg jeden raz na dobę.
Przypisy
- 1 2 3 Edoxaban, [w:] PubChem [online], United States National Library of Medicine, CID: 10280735 [dostęp 2020-10-31] (ang.).
- ↑ Safety Data Sheet. Edoxaban, Santa Cruz Biotechnology, 24 sierpnia 2015, SC-483508 [dostęp 2020-10-31] (ang.).
- 1 2 Savaysa (edoxaban) tablets for oral use [online], Agencja Żywności i Leków, 2015 [dostęp 2020-10-31].
- 1 2 3 4 5 6 7 8 9 10 11 12 13 Lixiana 15 mg tabletki powlekane. Charakterystyka Produktu Leczniczego, Daiichi Sankyo Europe, Europejska Agencja Leków [dostęp 2020-10-31].
- ↑ Jan Podlewski, Alicja Chwalibogowska-Podlewska, Encyklopedia Leki Współczesnej Terapii, wyd. XXII, Warszawa: Medical Tribune Polska, 2019, s. 320–321, ISBN 978-83-951310-6-6.
- ↑ WHO Model List of Essential Medicines 21th List [online], Światowa Organizacja Zdrowia, 2019 [dostęp 2020-10-31] (ang.).
- ↑ Obwieszczenie Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych z dnia 8 lipca 2020 r. w sprawie ogłoszenia Urzędowego Wykazu Produktów Leczniczych Dopuszczonych do Obrotu na terytorium Rzeczypospolitej Polskiej, „Dziennik Urzędowy Ministra Zdrowia”, 20 lipca 2020 [dostęp 2020-10-31].
![]() Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.