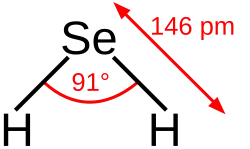
Selenowodór
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||
| Wzór sumaryczny |
H2Se | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
80,98 g/mol | ||||||||||||||||||||||||||
| Wygląd |
bezbarwny gaz o charakterystycznym zapachu zgniłego czosnku[1] | ||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||
Selenowodór, H
2Se – nieorganiczny związek chemiczny selenu i wodoru. Jest palnym, silnie trującym gazem o charakterystycznym, ostrym zapachu.
Właściwości
Słabo rozpuszcza się w wodzie (ok. 10 g/l), wodny roztwór zwany jest kwasem selenowodorowym, który jest dość słabym kwasem beztlenowym. Od selenowodoru wywodzą się sole – selenki. Selenowodór spala się w powietrzu do ditlenku selenu:
- 2H
2Se + 3O
2 → 2SeO
2 + 2H
2O
Otrzymywanie
- Synteza bezpośrednia w podwyższonej temperaturze z wodoru i selenu:
- H
2 + Se → H
2Se
- Działanie na selenki (np. cynku) kwasem solnym:
- ZnSe + 2HCl → H
2Se + ZnCl
2
Zagrożenia
Selenowodór jest silnie toksycznym gazem, bardziej od H
2S. Dawka 0,07 mg selenowodoru w 1 dm³ powietrza jest śmiertelna dla dorosłego człowieka. Selenowodór jest stosowany przy wytwarzaniu związków selenoorganicznych oraz selenków.
Przypisy
- 1 2 3 4 5 6 7 8 9 10 11 12 13 Hydrogen selenide, [w:] GESTIS-Stoffdatenbank [online], Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung, ZVG: 570243 [dostęp 2022-08-19] (niem. • ang.).
- ↑ Hydrogen selenide [online], karta charakterystyki produktu SIAD, 22 sierpnia 2017 [dostęp 2022-08-19] (ang.).
- ↑ Hydrogen selenide, [w:] ChemIDplus [online], United States National Library of Medicine [dostęp 2022-08-19] (ang.).
![]() Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.